翼思生物和STADA达成用于治疗帕金森病的药械产品合作
关注订阅预警->医药魔方Plus2022-03-18
2022年3月18日,中国上海和德国巴特菲尔伯尔,翼思生物(上海)与STADA集团旗下英国BRITANNIA公司签署一项独家许可协议,翼思获得用于治疗帕金森病的阿扑吗啡皮下注射液在中国大陆、香港和澳门开发和商业化权益。根据协议,BRITANNIA将获得首付款、里程碑式付款以及分级特许权使用费。

目前,中国约有300万人患有帕金森病,每年约有新增诊断15万人。Stacy等人(2008)做的一项注册研究发现,有16%的帕金森病人处于可以接受连续或间歇性多巴胺能手段治疗的中晚期阶段。全世界超过1万多名帕金森氏症患者正在使用阿扑吗啡。STADA, BRITANNIA和他们的合作伙伴向5大洲的29个国家提供多种商品名的阿扑吗啡产品。 翼思生物和STADA将在临床试验和其他获得注册上市批准要求的方面进行合作,将这种治疗方案提供给中国患者。阿扑吗啡皮下注射在2020版的中国帕金森病治疗指南中被推荐为一种治疗选择。
翼思生物首席执行官龙爱晶博士表示:“我们很高兴和BRITANNIA达成这项重要的战略合作。继小分子药物、创新非药物疗法之后,此次引进药械组合治疗性产品。这将进一步丰富翼思多元化的产品管线,更好地服务中枢神经疾病患者。”STADA集团首席执行官Peter Goldschmidt评论道:“此次与翼思生物的合作,开发并商业化帕金森病特定疗法,为STADA进入广阔和不断增长的中国医药市场提供了进一步的途径。为世界各地的患者提供新的治疗选择,是STADA作为值得信赖的合作伙伴关爱人类健康的宗旨。”BRITANNIA首席执行官Robert Wood说:“我们非常高兴与翼思生物签署本项协议。翼思作为专注于中枢神经领域的创新公司,拥有非常强的专业化团队,是阿扑吗啡皮下注射液在授权区域理想的开发和商业化合作伙伴。”
关于阿扑吗啡皮下注射液
帕金森病是一种常见的中老年神经系统退行性疾病,当前,随着人口老龄化,发病率正在逐步升高。随着疾病的进展,帕金森病的运动和非运动症状会逐渐加重,这会损害患者本身的日常活动,也会带来巨大的社会和医疗负担。
一项发表在《柳叶刀神经病学》杂志上关于阿扑吗啡皮下注射液3期临床研究——TOLEDO结果显示,与安慰剂相比,阿扑吗啡皮下注射治疗12周后,“关期”明显缩短:试验组每天缩短2.47个小时,安慰剂为0.58个小时,相差近2个小时(p=0.0025), “关期”缩短了一倍。阿扑吗啡皮下注射起效迅速,在治疗后的第一周内便可观察到结果。这些对帕金森病患者而言是有意义的临床试验终点。
阿扑吗啡皮下注射液包括一次性注射笔(PEN)和持续输注疗法(INFUSION)两个药械组合产品。阿扑吗啡是多巴胺D2受体激动剂,用于中晚期帕金森病运动症状的“开关”现象(ON-OFF)“关期“事件的治疗。阿扑吗啡皮下注射液已成功在全球多个国家上市,获得包括中国在内的多个国家和组织的帕金森病指南推荐。
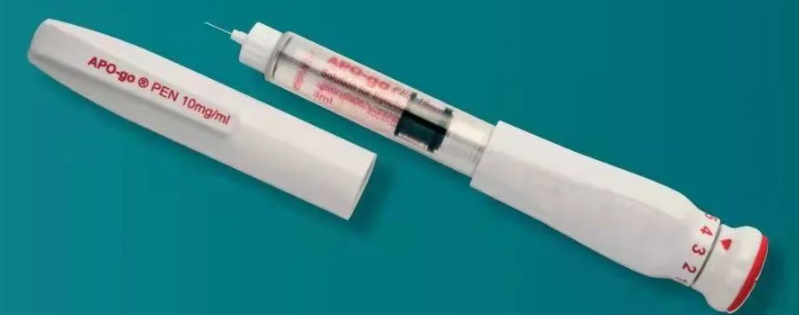
PEN是一种一次性、便携式注射笔,用于皮下注射阿扑吗啡,可绕过功能失调的胃肠道,为患者快速减少“关期”时间。

INFUSION由微型输注泵提供持续的阿扑吗啡皮下输注,可在不增加运动障碍的情况下显著减少“关期”时间,在临床上具有重要意义,是一种有效且耐受性良好的治疗策略。
-
阿扑吗啡
如需垂询请联系
hi@pharmacube.com